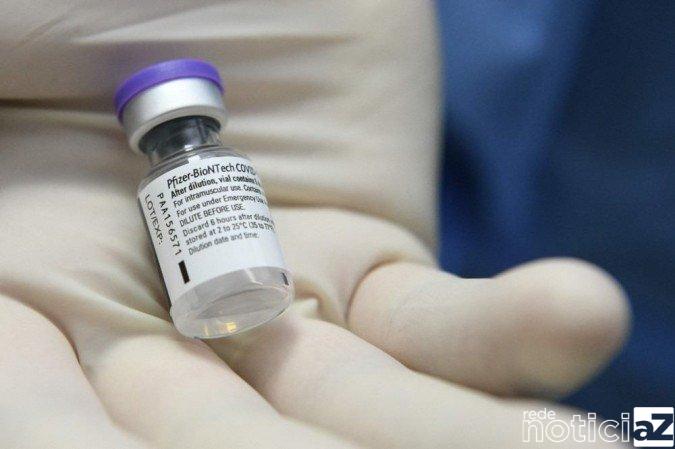

A vacina da Pfizer/BioNTech contra a Covid-19 mostrou eficácia em crianças de 5 a 11 anos. Segundo a farmacêutica dos Estados Unidos, o índice de proteção é de 90,7%. Todas as informações foram detalhadas para a Food and Drug Administration (agência regulatória americana).
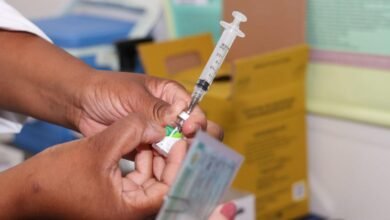
De acordo com a Pfizer, o estudo acompanhou 2.268 crianças de 5 a 11 anos que receberam duas doses da vacina ou placebo, com três semanas de intervalo. Cada dose foi um terço da quantidade administrada a adolescentes e adultos.
Segundo os pesquisadores, 16 crianças que receberam o placebo foram infectadas com Covid-19, em comparação com três que receberam o imunizante.
Em setembro, Pfizer e BioNTech anunciaram que a vacina é segura e induz resposta imune em crianças dessa faixa etária.
Vacina sendo ampliada para os mais novos
O governo norte-americano quer ampliar a vacinação contra a Covid-19 para as crianças e para isso detalhou o plano de imunização. Caso haja uma aprovação do imunizante, o plano é que “seja distribuída rapidamente e disponibilizada conveniente e igualitariamente a famílias de todo o país”, disse a Casa Branca em um comunicado. Assim as outras agências reguladoras estudarão a aprovação de maneira independente.
No Brasil, a vacina da Pfizer pode ser aplicada em adolescentes a partir de 12 anos. Em junho, a Agência Nacional de Vigilância Sanitária (Anvisa) autorizou o uso do imunizante nessa faixa etária e, em setembro, após um vai e vem, o Ministério da Saúde voltou a liberar a vacinação de adolescentes de 12 a 17 anos, mesmo os sem comorbidades, contra a Covid-19.
Terceira dose
Para evitar o risco de contágio da variante delta do coronavírus, a terceira dose ou dose de reforço estão sendo aplicadas. E o imunizante da Pfizer garante uma proteção de 95,6%, segundo um estudo feito em 10 mil pessoas com 16 anos ou mais.
De acordo com o comunicado, as companhias afirmaram que esse resultado foi obtido durante um período em que a variante delta já era a dominante. Com esses dados, que ainda não foram publicados em uma revista científica revisada por pares, os executivos do consórcio pretendem obter autorização de agências reguladoras para o licenciamento do reforço para qualquer pessoa que tenha tomado as duas doses anteriores.
Todos os participantes do ensaio de fase 3 haviam recebido as duas doses antes e foram divididos em grupos aleatórios: metade teve o reforço 11 meses depois da segunda aplicação, enquanto os demais foram inseridos no braço de placebo. A ocorrência de covid-19 com sintomas foi acompanhada, em média, por dois meses e meio. Nesse período, houve cinco casos no grupo do reforço e 109 no placebo, o que significa uma eficácia relativa de 95,6%.
A idade média dos participantes foi de 53 anos, com 55,5% deles entre 16 e 55 e 23,3% acima dos 65. Segundo o comunicado, as análises de subgrupos mostraram que os resultados foram iguais, independentemente de idade, sexo, raça, etnia ou comorbidades. A Pfizer e a BioNTech afirmaram que esses são os primeiros resultados de eficácia da dose de reforço em um ensaio randomizado (que inclui o grupo de placebo) e controlado.
LEIA TAMBÉM
Intervalo da CoronaVac entre as duas doses é reduzido para 15 dias